
近日,金沙2004路线js5生物医学工程研究室曾烨副研究员团队在抗肿瘤血管形成研究方面取得突破性进展,相关研究成果“Anti-angiogenesis triggers exosomes release from endothelial cells to promote tumor vasculogenesis”发表于国际胞外囊泡协会(The International Society for Extracellular Vesicles,ISEV)会刊Journal of Extracellular Vesicles(胞外囊泡杂志,影响因子11)上。该研究论文第一作者为曾烨副研究员,通讯作者为曾烨副研究员和美国纽约城市大学Bingmei M.Fu教授,金沙2004路线js5为第一单位。金沙2004路线js5刘肖珩研究员、李良研究员、刘小菁研究员、吴江研究员、何学令副研究员等也参与了本项目研究。
抗血管生成疗法(anti-angiogenic therapies,AATs)被用于多种恶性肿瘤的治疗,其临床疗效因继发性的肿瘤血管形成(vasculogenesis)和肿瘤生长而受限。研究揭示了AATs治疗后肿瘤血管形成和肿瘤生长的分子机制。研究首先将微小RNA-9(microRNA-9, miR-9)转染至人脐静脉内皮细胞,以模拟肝癌中的肿瘤相关性内皮细胞,探讨AATs对内皮细胞的影响及其作用机制。研究发现,miR-9诱导血管生成。抗血管生成的抑制剂凡德他尼(vandetanib)完全抑制了miR-9诱导的血管生成(angiogenesis),并促进了人脐静脉内皮细胞的自噬,同时,还诱导了富血管内皮生长因子(vascular endothelial growth factor,VEGF)外泌体的释放。
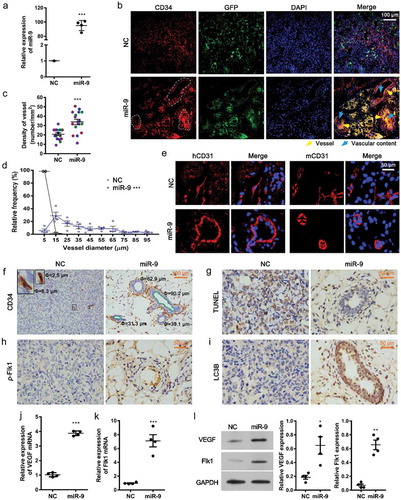
图miR-9促进血管生成
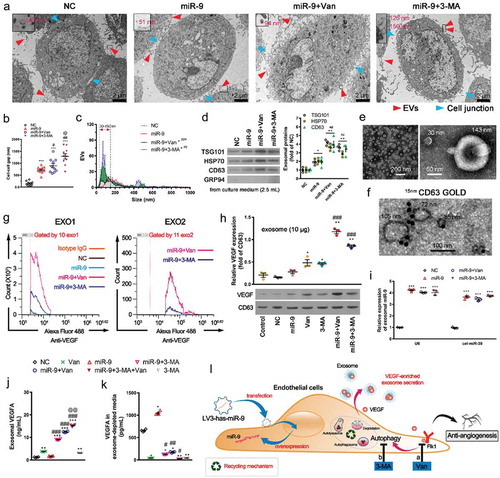
图AATs或抗自噬促进人脐静脉内皮细胞释放富VEGF外泌体
该工作首次报道了富VEGF外泌体可显著促进内皮血管生成和肝癌细胞血管生成拟态,促进肝癌在裸鼠体内的生长。抗自噬也可以抑制血管内皮细胞的血管生成,但是与AATs相似,自噬抑制剂3-MA促进了富VEGF外泌体的释放。体外实验还表明,抑制外泌体的释放,或使用VEGF中和性抗体处理富VEGF外泌体,可以显著抑制肿瘤细胞的血管生成拟态。由此可见,AATs和抗自噬后的肿瘤血管形成和肿瘤生长是内皮细胞和肿瘤细胞相互作用的结果,由富VEGF的外泌体所介导。
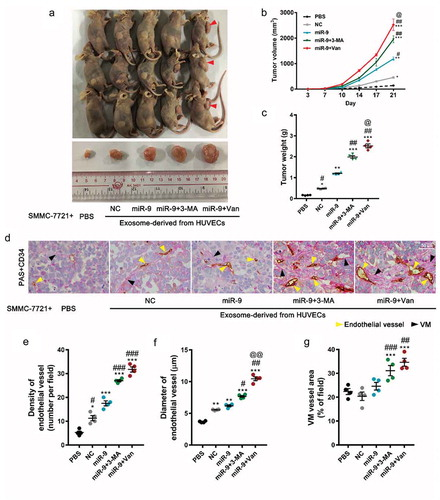
图富VEGF外泌体促进肿瘤生长和血管形成
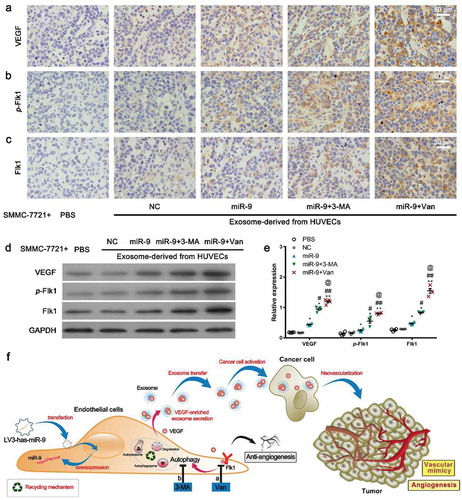
图富VEGF外泌体激活血管形成信号通路
f.血管内皮细胞释放富VEGF外泌体促进肿瘤血管形成的机制
该工作发现的AATs或抗自噬治疗后,肿瘤相关性内皮细胞分泌富VEGF外泌体进而促进肿瘤血管形成的现象,为AATs后补偿性血管形成提供了一个合理的解释。抗自噬较AATs释放更少的富VEGF外泌体,说明抗自噬可成为AATs的辅助或替代性治疗手段,以更有效地抑制肿瘤血管形成。本工作所提出的富VEGF外泌体生成及其作用机制,为开发肿瘤的长效抗血管和抗自噬治疗药物提供了新策略。
Ye Zeng, Xinghong Yao, Xiaoheng Liu, Xueling He, Liang Li, Xiaojing Liu, Zhiping Yan, Jiang Wu & Bingmei M. Fu (2019) Anti-angiogenesis triggers exosomes release from endothelial cells to promote tumor vasculogenesis, Journal of Extracellular Vesicles, 8:1, 1629865, DOI: 10.1080/20013078.2019.1629865.
原文链接:
https://www.tandfonline.com/doi/full/10.1080/20013078.2019.1629865